救急外来での対応
・外傷、事故の有無の確認
・まずは頭蓋内損傷、脳卒中、急性心筋梗塞の除外
・低血糖の除外(→ 血糖測定)
※大量飲酒によるエタノール代謝によって、NADH/NAD比が減少し、ピルビン酸→乳酸の反応が進み、肝臓での糖新生が阻害されるためである。
※特に慢性アルコール依存の患者では、食事量低下のため肝臓に蓄えられているグリコーゲンが少なく、食事を摂取せずに飲酒をするため低血糖を起こしやすい。
診察
・慢性肝障害の所見の確認
手掌紅斑、クモ状血管腫、腹水、女性化乳房の有無
検査
・血糖:必ず!
・ビタミンB1、アンモニア(意識障害があれば)
処置
・意識障害時、低血糖がなければビタミンB1静注
アリナミンF®20mL(100mg) 1~2本緩徐静注
(リメファー3B 1A中、ビタミンB1 100mg)
① アルコール性低血糖
・大量飲酒によるエタノール代謝によって、NADH/NAD比が減少し、ピルビン酸→乳酸の反応が進み、肝臓での糖新生が阻害されるためである。
・特に慢性アルコール依存の患者では、食事量低下のため肝臓に蓄えられているグリコーゲンが少なく、食事を摂取せずに飲酒をするため低血糖を起こしやすい。
機序
参照(このサイトより引用):https://double-cradle.jp/diabetes-mellitus-knowledge/signs-and-symptoms/pathogenic-mechanism-of-alcoholic-hypoglycemia.html)
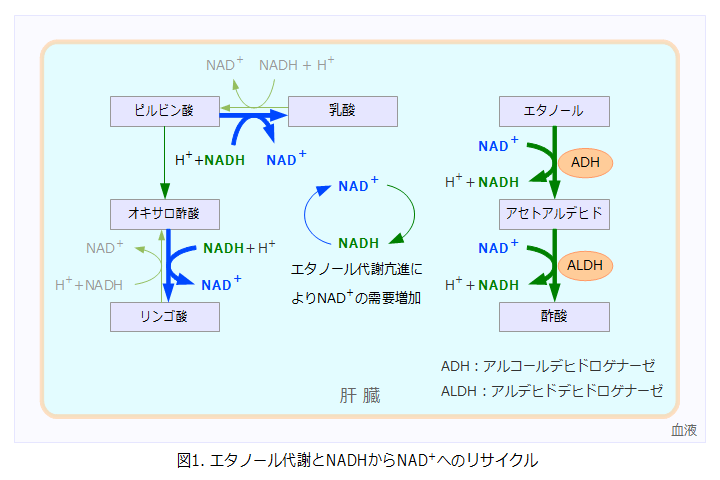
エタノールが酸化されてアセトアルデヒドになる反応は、酵素アルコールデヒドロゲナーゼ(アルコール脱水素酵素)によって触媒される。その際に補酵素NAD+(nicotinamide adenine dinucleotide)も必要。
アセトアルデヒドから酢酸への反応も、酵素アルデヒドデヒドロゲナーゼ(アルデヒド脱水素酵素)によって触媒される際に、補酵素NAD+が使われる。
↓
長期的なアルコール摂取により、肝ミトコンドリアにNADHが蓄積し、NADH/NAD比が高まる
↓
ピルビン酸がNADHで還元されて乳酸とNAD+が生成する方向に傾く(→乳酸アシドーシス)
↓
NADH/NAD比が上昇することで,糖新生やTCA回路が抑制される。
このエタノール代謝過程で肝グリコーゲンが消費されるため,肝グリコーゲン貯蔵量が減少する。
↓
低血糖
② 急性アルコール中毒
・飲酒量と飲酒速度の確認
・アルコール臭の確認
浸透圧ギャップによる予測アルコール血中濃度の計算
・Na、BUN、ブドウ糖以外の浸透圧活性をもった溶質が存在すると血漿浸透圧の測定値は計算値よりも大きくなる(正常OG:1.9±3.7mOsm/L)
・浸透圧ギャップ(osmolar gap:OG)
=浸透圧測定値ー{2Na+(BUN/2.8)+(BS/18)}
・予測アルコール濃度=浸透圧ギャップ×4.6
(軽度:20~150、中等度:150~300、重度>300)
③ Wernicke(ウェルニッケ)脳症
・ビタミンB1(チアミン)欠乏症による急性代謝性脳症
・アルコールによるビタミンB1吸収率低下、肝機能障害によるビタミンB1活性化障害、栄養不良などが原因
※ ビタミンB1は主に糖質と分枝鎖アミノ酸代謝での補酵素として働くため、高炭水化物食やアルコール多飲で欠乏しやすい
※ ビタミンB1を多く含む食品:サーモン、アーモンド、豚肉など
機序
・ビタミンB1 は解糖系やTCAサイクルの補酵素として糖代謝に重要である。
・ビタミンB1 は解糖系の最終代謝産物であるピルビン酸をアセチルCoAに変換するピルビン酸デヒドロゲナーゼ複合体の補酵素の原料である。
・その欠乏によりピルビン酸がTCAサイクルに進まず、好気的ATP産生ができなくなり、細胞活動のエネルギーが枯渇する。
・さらにピルビン酸は乳酸となり、乳酸アシドーシスを引き起こす
・健常人の1日のビタミンB1必要量は1~2mgといわれている。体内に貯蔵されている量は30~50mgしかないため、摂取しなければ2~7週間で枯渇してしまう。
症状
古典的3徴:
「小脳性運動失調」
「外眼筋麻痺」(水平性眼振と外転不全が多い。両側眼球が内下方に寄る(ウルトラマンの黒目))
・3徴が揃うことは稀で、多くは軽い意識障害のみ
・最も多いのは亜急性の意識変容(53%)
・眼症状で多いのは眼振(85%)、外転神経麻痺(54%)
・末梢血管拡張と静脈還流増加による、wet beriberiとわれる高拍出性心不全を来す(機序は不明)
・死亡率は10~20%
参照:Caine criteria
2つ以上で陽性(感度83%)→治療開始
「Dr.林の『MEAL』」
M:mulnutirition(栄養失調)
E:eye movement disturbance(眼球運動障害)
A:ataxia(小脳失調)
L:level of consciousness(意識障害、軽度記銘力障害)
検査所見
・MRI T2WI、DWIにて、第3脳室周囲視床内側部、中脳水道周囲、第4脳室底、乳頭体に高信号域
・血清ビタミンB1検査の感度と特異度は不明
→症状と身体所見から疑い、治療することが重要。
治療
※ブドウ糖をチアミンの前に投与すると症状が悪化するので注意(前か同時に投与)
静注、点滴治療
まず100㎎ワンショット投与。
半減期が短いため、1日2~3回投与(最低1日500㎎)
例)
・アリナミンF®(100mg/20mL)、メタボリン®(50mg/1mL)
(リメファー3B(1A内にビタミンB1 100㎎)でも代用可)
まず100㎎ 10分かけて点滴静注
・その後、1回200~500㎎ 1日3回10分かけて点滴静注 / 3日間
↓
その後 250㎎ 1日1回静注 / 5日間
↓
例)
ビタメジン配合カプセルB25(ビタミンB1 25㎎含有)
1回1C 1日3回 /20~30日間
・眼球運動障害は数時間で改善する
・小脳失調は数日間、意識障害は数週間程度かかることが多い
・画像所見は改善する
参照:
④ アルコール性ケトアシドーシス
参考:https://www.jmedj.co.jp/journal/paper/detail.php?id=7981
・慢性アルコール依存患者が大量飲酒を契機に発症することが多い
参考:AKA発症の機序
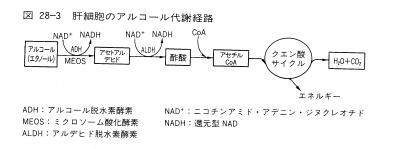
・長期的なアルコール摂取により肝ミトコンドリアにNADHが蓄積するため,NADH/NAD比が高まる。
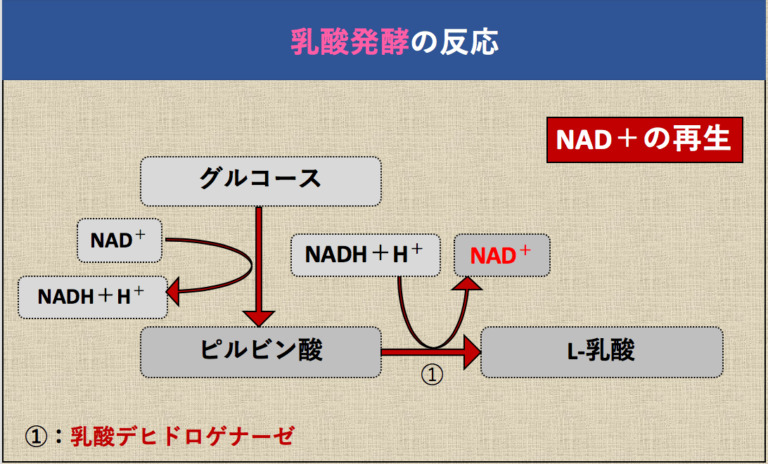
・NADH/NAD比が高い状態ではアセト酢酸(acetoacetic acid;ACAC)がβ–ヒドロキシ酪酸(3–OHBA)に代謝されやすいため,AKAに特徴的な3–OHBA/ACAC比の上昇をもたらす。
・一般的には,アルコール依存症患者が大量飲酒後に消化器症状により飲酒すらもできなくなる、といったような典型的な病歴
・ここで重要なのは除外診断であり、アニオンギャップ開大性の代謝性アシドーシスを呈する疾患を除外する必要がある。
⑤ アルコール離脱症候群
・アルコール依存患者の急激なアルコール中断や減量による脱抑制から生じる症状。
アルコール離脱症候群の症状
小離脱:断酒の6~24時間以内に出現
① 自律神経症状(交感神経興奮症状):手指振戦、発汗、頻脈、血圧上昇、発熱、皮膚紅潮
② 消化器症状:嘔気、嘔吐
③ 精神症状:不眠、不安、イライラ、集中力低下
・24時間後から小離脱顕在化
・48時間以内に「離脱けいれん」が出現(全身痙攣で左右差なし)
予測指示(例)
不眠、ふるえ、イライラ時
ジアゼパム(セルシン®ホリゾン®) 1回5㎎ 30分以上あけて計3回まで
小離脱出現後の指示
ジアゼパム(セルシン®ホリゾン®)1回5㎎ 1日3回 3日間、
その後1回2㎎ 1日3回に減量
(肝障害がある場合はその半量)
大離脱(振戦せん妄):
・離脱せん妄が出現する
・断酒の48時間~72時間後に出現
・無治療なら5~33%が死亡する!
・症状
・幻覚(体感幻覚、幻聴、幻視)小動物幻視
・交感神経興奮(高血圧、頻脈、焦燥)
・不眠
・嘔気・嘔吐
・振戦せん妄
・振戦、発汗、痙攣
予防・治療
・アルコールと同様にGABAの働きを増強させるベンゾジアゼピン(セルシン、ホリゾン)を選択する(脳内でベンゾジアゼピン受容体作動薬とエタノール作用部位が近いため、交叉耐性があるため、ベンゾジアゼピンがエタノール作用を補う)
・10㎎ iv、15分後効果判定、不十分なら10㎎追加iv、15分後効果判定(1時間で40㎎以上必要なら「治療抵抗性」)
 レジデントノート 2022年3月 Vol.23 No.18 一般外来 処方ドリル〜症例で鍛える! 慢性疾患・コモンプロブレムへの上手な薬の選び方・使い方
レジデントノート 2022年3月 Vol.23 No.18 一般外来 処方ドリル〜症例で鍛える! 慢性疾患・コモンプロブレムへの上手な薬の選び方・使い方



コメント