起因菌
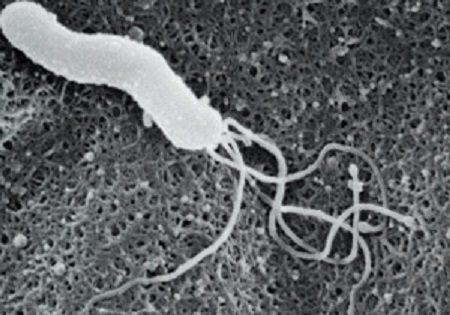
ヘリコバクター・ピロリ菌(Helicobacter pylori;H. pylori)
・らせん状グラム陰性桿菌
・数本の鞭毛を有する
・強力なウレアーゼ活性を持ち、尿素をアンモニアと二酸化炭素に分解することで周囲の胃酸を中和することで生息している
ヘリコバクター・ピロリ感染症(ドック学会専門医試験):
ヘリコバクター・ピロリ感染症について(ドック学会専門医試験):
・ヘリコバクター・ピロリ関連潰瘍は、胃角部から胃体部に多い。
・一方、NSAIDsによる潰瘍は胃幽門部(前庭部)に多い。
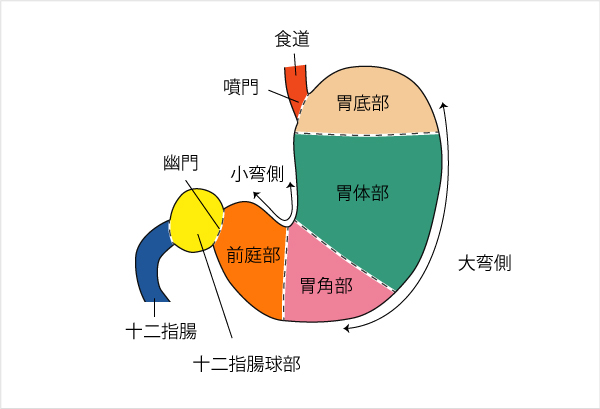
・ヘリコバクター・ピロリ除菌治療成功例に対して、潰瘍再発予防に抗潰瘍剤投与は必要ないとされている。
・ヘリコバクター・ピロリ除菌治療後の再陽性化率は(再感染化率)は年率2%以下と少ない。
・一方、NSAIDsを服用して酸分泌抑制をしないとき、胃潰瘍の再発率は10~15%である。
・ヘリコバクター・ピロリ抗体検査の検体は血液または尿を用いる。
病態
・感染経路として、古くは人の糞便が堆肥溜めから地下水に浸透し、井戸水からの感染とされていたが、現在の主な感染経路は、幼児期に近親者からの口移しなどによる家族内感染とされている。
・幼児期は胃酸の分泌能が低いため、経口感染がおこりやすい
・医療・介護従事者での感染も多い
・感染しているほぼすべての人に胃の炎症(胃炎)がみられ、胃炎は胃全体に広がっていることもあれば、胃の下部(胃前庭部)だけの場合もある。
・ピロリ菌 は胃酸の分泌を増やし、胃酸に対する正常な胃の防御機能を損ない、毒素を産生することで、胃潰瘍が形成される一因となる。
・またピロリ菌(H. pylori)感染が長期に及ぶと萎縮性胃炎を経て、胃癌のリスクが高まる(参照:萎縮性胃炎)
・鉄欠乏性貧血、慢性特発性血小板減少性紫斑病、慢性腎不全の原因にもなる
・除菌治療後の再感染率は0.2% / 年
ピロリ感染症と関連のある疾患
皮膚疾患
・慢性蕁麻疹
消化管疾患
・胃潰瘍
胃角部から胃体部に多い(↔NSAID潰瘍は胃幽門部(前庭部)に多い)
・十二指腸潰瘍
・萎縮性胃炎
・機能性ディスペプシ
・胃過形成性ポリープ
・胃MALTリンパ腫
・逆流性食道炎
血液疾患とピロリ感染症
特発性血小板減少性紫斑病(ITP)
・ITPは明らかな基礎疾患が無く、血小板数が減少するため種々の出血症状をひき起こす疾患。
・血小板に対する自己抗体ができて、脾臓で破壊されるために、数が減少すると考えられている。
・ピロリ菌陽性のITP患者にピロリの除菌治療を行うと血小板数が増加することが相次いで報告されている。
鉄欠乏性貧血
・IDAの原因として慢性消化管出血、婦人科出血、鉄吸収障害などがあるが、消化管内視鏡やエコー、CT等で調べても、約30%は原因不明で、鉄剤治療をしても再増悪を繰り返すことがある。
・こうした原因不明のIDAでピロリ菌陽性の患者さんに除菌療法を行うと、貧血が治ったという報告が増えている。
胃X線検査所見
・胃の粘膜が萎縮し粗雑に見える
・粘膜ヒダが太くなっている
(これらは除菌治療により改善する)
上部消化管内視鏡検査
「胃炎の京都分類」
・19の特徴的な内視鏡所見からH. pylori感染を「未感染」「現感染」「除菌後を含む既感染」に分類し、その組織学的胃炎の診断までをほぼ可能とした胃炎分類
・内視鏡検査で「現感染疑い」の患者に対して、ピロリ菌検査を提案する
① 鳥肌状胃炎
・胃粘膜に均一な小顆粒状隆起が密集して認められるもの
・若年者、感染早期に認められる
・未分化癌の発生母地として注目されている
・除菌により軽快する
② 萎縮性胃炎
・白色調の連続する粘膜下に樹枝状の血管が透けて見える
・ピロリ感染が慢性化した状態
③ 黄色腫
・白色~黄色調の丈の低い隆起性病変で、細顆粒状の表面構造
・ピロリ菌による高度の炎症に起因して発生する
診断法
ヘリコバクター・ピロリの感染診断:
・保険適応上は6種類の検査が認められている
1)侵襲的検査法(内視鏡の胃生検材料を用いる方法)
① 迅速ウレアーゼ試験
・ピロリ菌のウレアーゼ活性によって尿素から弱アルカリ性のアンモニアが産生されることを利用して、pH指示薬の色の変化から診断する。
② 組織生検法
・胃粘膜生検病理組織にてピロリ菌を観察する方法
③ 培養法
・薬剤感受性を調べる時に必要
2)非侵襲的診断法(内視鏡下での胃生検を用いない方法)
① 尿素呼気試験
・感度、特異度ともに90%以上であり第一選択
・ピロリ菌のウレアーゼ活性により尿素から二酸化炭素が産生されることを利用した検出法
・非放射性同位元素である13Cでラベルした尿素を胃内で反応させ、ピロリ菌のウレアーゼがある場合は尿素が分解され、ラベルされたCO2が呼気中に検出されることを利用している。
・すでにPPIなどの胃酸抑制薬を服用している場合は偽陰性となるため、少なくとも2週間以上の休薬が必要
② 抗体検査
・すでにPPIやP-CABをを服用している場合でも可
・血清または尿を用いた検査法
・感染が終息しても抗体は徐々に減少するため、数年にわたって抗体が陽性域に留まることがある(偽陽性)
③ 便中抗原検査
・すでにPPIやP-CABを服用している場合でも可能
※「便中抗原検査」や「血清抗体検査」は特異度が低いため、偽陽性が多く出てしまう
→これらはスクリーニングには使用しないこと
除菌治療
※ 除菌により、胃がん発生を減らすことができる(しかし総死亡は減らない)。
1次除菌(除菌率70~80%)
ボノサップパック®(400)
・タケキャブ(20㎎) 1回1錠 1日2回
・サワシリン(250㎎) 1回3錠 1日2回(アモキシシリンAMPC)
・クラリス(200㎎) 1回1錠 1日2回
※ 1日1シートを朝夕食後の2回に分けて内服 / 7日間
参考(このサイトより引用):https://www.otsuka-elibrary.jp/product/di/bn4/photo/index.html

2次除菌
・ボノピオンパック 1日1シートを朝夕食後の2回に分服 / 7日間
副作用(全体の約50%にみとめる)
・水様下痢、軟便(10~30%)
・味覚異常
・皮疹(2~5%)
・出血性腸炎(ごくまれ)
※ 整腸剤は治療副作用である下痢症状を抑えるのみならず、除菌効果自体も高めることが報告されており、併用を検討してもよい。
効果判定
・除菌判定には、その感度と特異度の高さから、尿素呼気試験が最も推奨される。
・完全にピロリ菌が除菌できたことを確認するため、薬剤の使用終了から4週間以上経過して除菌判定を行うことが必要である(プロトンポンプ阻害薬(PPI)などの静菌作用を有する薬剤の使用は感染診断に際し偽陰性を示すことがあるため)。
・治療後の効果判定検査は内服終了後4週間以上あけて検査する。
・尿素呼気試験が第一選択、ついで便中抗原検査
除菌後の対応
・再感染率は年0.5%(2%以下)
・正常粘膜と比較して胃癌発生リスクがあるため(萎縮性胃炎:OR2.8、腸上皮化生:OR 3.4)、1~2年毎の内視鏡検査を勧める(ガイドラインでは年齢による上限に決まりはない)
・特に高度の萎縮性胃炎では毎年の内視鏡フォローが必要
・除菌成功例に潰瘍再発予防に抗潰瘍剤投与は不要である
参考:胃がんリスク判定(ABC分類)
・採血で「ピロリ菌抗体検査」と「血清ペプシノーゲン検査(PG検査)」を行い、その組み合わせで、胃がん発症のリスクを判定するもの。
血清ペプシノーゲン検査(PG検査)
・ペプシノーゲン(以下PG)は胃液に含まれる消化酵素ペプシンの前駆物質で、胃内に分泌される。
・胃粘膜萎縮が進行すると血中ペプシノゲン値が低下する。つまり血中ペプシノゲンが低下していれば、胃の粘膜の萎縮が進んでいることがわかります。
・さらにペプシノゲンには主に胃底腺から分泌されるペプシノゲンI(PGⅠ)と、胃底腺だけではなく、噴門腺や幽門腺、十二指腸腺からも分泌されるペプシノゲンII(PGⅡ)の2種類がある。
・胃粘膜の萎縮が進行すると,胃底腺領域は萎縮し幽門線領域が拡張することから,ペプシノゲンⅠに対しペプシノゲンⅡが相対的に増加するため,ペプシノゲンⅠ/Ⅱ比が低下する。
・ペプシノゲンⅠ/Ⅱ比は,胃粘膜の萎縮を伴う疾患において有意に低下することから,ペプシノゲンⅠ値,ペプシノゲンⅠ/Ⅱ比の組み合わせによる解析は,消化性潰瘍,萎縮性胃炎,胃癌高危険群のスクリーニングの補助等に有用と考えられている。
血清ペプシノゲン値(PG値)のカットオフ値
・血中ペプシノゲン量が少ない場合が陽性で、胃粘膜が萎縮していることを示す。
・血清ペプシノゲン値(PG値)はPGⅠ≦70かつPGⅠ/Ⅱ≦3を陽性(+)のカットオフ値とする
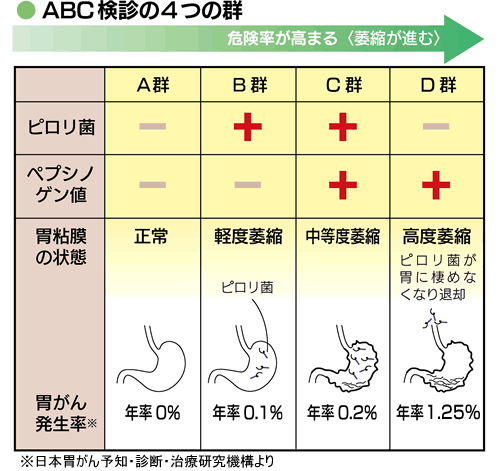
ABC分類
・胃がんの発症リスクの度合いに応じてA・B・C・Dに分類・判定をする検診方法
・胃がんの発症リスクは、D群>C群>B群>A群の順に高くなる
・検査の結果、B群・C群・D群の判定を受けた人は、内視鏡検査を受けて胃の状態を確認し、尿素呼気試験等でピロリ菌感染が認められた場合は、除菌治療を受けてもらう
判定
A群:ピロリ菌抗体(-)PG検査(-)
ピロリ菌に未感染で萎縮がなく、将来胃がん発症リスクのほとんどない人
B群:ピロリ菌抗体(+)PG検査(-)
ピロリ菌に感染していて、萎縮のない(もしくは軽度)の人で、将来胃がん発症リスクのある人
C群:ピロリ菌抗体(+)PG検査(+)
ピロリ菌感染により胃粘膜の萎縮がある人で、将来胃がん発症リスクの高い人
D群:ピロリ菌検査(-)PG検査(+)
ピロリ菌感染により胃の粘膜の萎縮が高度に進んだために、ピロリ菌が胃に住めなくなった人で、将来胃がん発症リスクの最も高い人(ピロリ菌既感染)

ヘリコバクター・ピロリ関連潰瘍
・胃潰瘍は胃角部から胃体部に多い(↔NSAID潰瘍は胃幽門部(前庭部)に多い)
・除菌後は潰瘍再発予防に抗潰瘍薬投与は必要なし
特集 あなたの切実なギモンにズバリ答えます! 消化器診療“虎の巻”


コメント